



При сгорании 5,92 г вещества А, содержащего 43,24 % кислорода по массе, получено 4,24 г карбоната натрия и 1,792 л углекислого газа (н.у.). Вещество А образуется при нагревании вещества Б с водным раствором гидроксида натрия, причём вторым продуктом реакции является этанол.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим массу и количество кислорода в веществе А:
m(O) = 5,92 · 0,4324 = 2,56 г
n(O) = 2,56 / 16 = 0,16 моль
Шаг 2. Находим количество карбоната натрия:
n(Na2CO3) = 4,24 / 106 = 0,04 моль
Следовательно, n(Na) = 2 · 0,04 = 0,08 моль, m(Na) = 0,08 · 23 = 1,84 г
Шаг 3. Находим количество CO2:
n(CO2) = 1,792 / 22,4 = 0,08 моль
Шаг 4. Общее количество углерода складывается из углерода в CO2 и в Na2CO3:
n(C из CO2) = n(CO2) = 0,08 моль
n(C из Na2CO3) = n(Na2CO3) = 0,04 моль
nобщ.(C) = 0,08 + 0,04 = 0,12 моль
m(C) = 0,12 · 12 = 1,44 г
Шаг 5. Находим массу и количество водорода по разности:
m(H) = 5,92 − 1,44 − 2,56 − 1,84 = 0,08 г
n(H) = 0,08 / 1 = 0,08 моль
Шаг 6. Находим соотношение:
n(C) : n(H) : n(O) : n(Na) = 0,12 : 0,08 : 0,16 : 0,08 = 3 : 2 : 4 : 2
Молекулярная формула: C3H2O4Na2, M = 36 + 2 + 64 + 46 = 148 г/моль
Шаг 7. Определяем структуру. Вещество А — натриевая соль с двумя атомами Na и четырьмя атомами кислорода, следовательно это соль двухосновной кислоты с двумя группами COONa. На углеродный скелет остаётся 1 атом C (3 − 2 = 1) и 2 атома H. Это группа CH2.
Вещество А — динатриевая соль пропандиовой кислоты:
NaOOC–CH2–COONa
Шаг 8. Вещество Б при нагревании с NaOH даёт вещество А и этанол, следовательно Б — диэтиловый эфир пропандиовой кислоты:
Вещество А состава CxHxOxKy содержит 33,0 % кислорода по массе. Известно, что 4,85 г вещества А можно получить при взаимодействии кислородсодержащего органического вещества Б с раствором, содержащим 5,0 г гидрокарбоната калия, причём эти вещества взаимодействуют в молярном соотношении 1:2.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим количество KHCO3:
n(KHCO3) = 5,0 / 100 = 0,05 моль
Шаг 2. Вещество Б реагирует с гидрокарбонатом калия, следовательно Б — карбоновая кислота, реакция — нейтрализация. Из соотношения 1:2:
n(Б) = 0,05 / 2 = 0,025 моль
n(A) = n(Б) = 0,025 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 4,85 / 0,025 = 194 г/моль
Шаг 4. Находим x из массовой доли кислорода. Формула CxHxOxKy:
ω(O) = 16x / 194 = 0,33
16x = 64
x = 4
Шаг 5. Находим y:
M(A) = 12x + x + 16x + 39y = 194
12·4 + 4 + 16·4 + 39y = 194
48 + 4 + 64 + 39y = 194
39y = 78
y = 2
Молекулярная формула: C4H4O4K2, M = 194 г/моль
Дополнительная проверка: y = 2 согласуется с тем, что вещество Б реагирует с KHCO3 в соотношении 1:2 (двухосновная кислота).
Шаг 6. Определяем структуру. Два атома K и четыре атома O — это две группы COOK. На скелет остаётся 2 атома C и 4 атома H. Это фрагмент –CH2–CH2–.
Вещество А — дикалиевая соль бутандиовой кислоты:
KOOC–CH2–CH2–COOK
Шаг 7. Вещество Б — бутандиовая кислота:
HOOC–CH2–CH2–COOH + 2KHCO3 → KOOC–CH2–CH2–COOK + 2H2O + 2CO2↑
Вещество А состава CxH2x+1O2yN2yKy содержит 17,4% кислорода по массе. Известно, что 4,60 г вещества А можно получить при взаимодействии кислородсодержащего органического вещества Б с раствором, содержащим 1,40 г гидроксида калия, причём эти вещества взаимодействуют в молярном соотношении 1:1. Молекула вещества Б имеет неразветвлённый углеродный скелет, содержит три функциональные группы, при этом азотсодержащие функциональные группы максимально удалены друг от друга.
На основании данных условия задания:
1) проведите необходимые вычисления и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связей атомов в его молекуле;
3) напишите уравнение получения вещества А при взаимодействии вещества Б с гидроксидом калия (используйте структурные формулы органических веществ).
Шаг 1. Находим количество KOH:
n(KOH) = 1,40 / 56 = 0,025 моль
Шаг 2. Из соотношения 1:1:
n(Б) = n(KOH) = 0,025 моль
n(A) = n(Б) = 0,025 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 4,60 / 0,025 = 184 г/моль
Шаг 4. Находим y из массовой доли кислорода. Формула CxH2x+1O2yN2yKy:
ω(O) = 16·2y / 184 = 0,174
32y = 32
y = 1
Следовательно в молекуле 2 атома O, 2 атома N, 1 атом K.
Шаг 5. Находим x:
M(A) = 12x + 2x + 1 + 32 + 28 + 39 = 184
14x + 100 = 184
14x = 84
x = 6
Молекулярная формула: C6H13O2N2K, M = 72 + 13 + 32 + 28 + 39 = 184 г/моль
Шаг 6. Определяем структуру. Вещество Б реагирует с KOH в соотношении 1:1, следовательно в молекуле одна группа COOH (2 атома O и 1 атом K в соли). Два атома N — это две группы NH2. Итого три функциональные группы: COOH + 2 NH2.
Неразветвлённый скелет из 6 атомов C, азотсодержащие группы максимально удалены друг от друга:
Вещество А — калиевая соль 2,6-диаминогексановой кислоты:
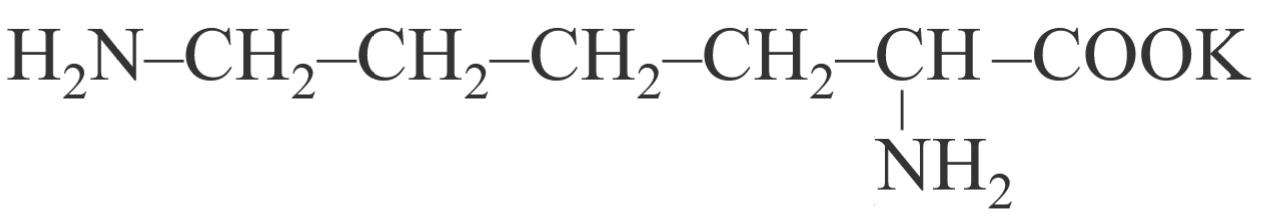
Шаг 7. Уравнение реакции:
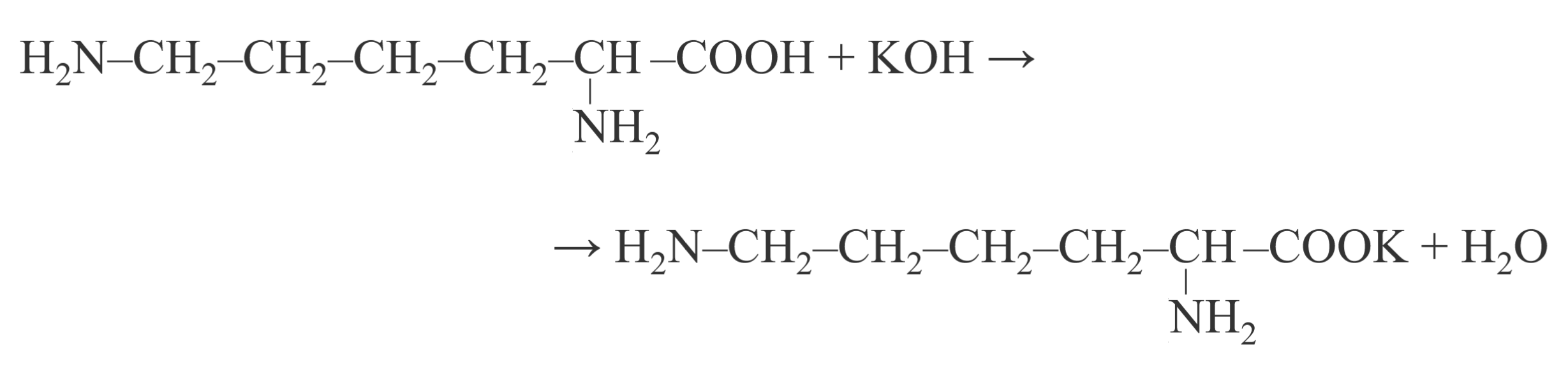
При сгорании 10,8 г органического вещества А, содержащего 29,6% кислорода, получили 7,84 л углекислого газа (н.у.), 5,3 г карбоната натрия и воду. Известно, что заместители в структуре вещества А максимально удалены друг от друга. При нагревании вещества А с гидроксидом натрия образуется вещество Б, молекула которого содержит только вторичные атомы углерода и не содержит π-связей.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с гидроксидом натрия с получением вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим массу и количество кислорода в веществе А:
m(O) = 10,8 · 0,296 = 3,2 г
n(O) = 3,2 / 16 = 0,2 моль
Шаг 2. Находим количество карбоната натрия:
n(Na2CO3) = 5,3 / 106 = 0,05 моль
Следовательно, n(Na) = 2 · 0,05 = 0,1 моль, m(Na) = 0,1 · 23 = 2,3 г
Шаг 3. Находим количество CO2:
n(CO2) = 7,84 / 22,4 = 0,35 моль
Шаг 4. Общее количество углерода складывается из углерода в CO2 и в Na2CO3:
n(C из CO2) = n(CO2) = 0,35 моль
n(C из Na2CO3) = n(Na2CO3) = 0,05 моль
nобщ.(C) = 0,35 + 0,05 = 0,4 моль
m(C) = 0,4 · 12 = 4,8 г
Шаг 5. Находим массу и количество водорода по разности:
m(H) = 10,8 − 4,8 − 3,2 − 2,3 = 0,5 г
n(H) = 0,5 / 1 = 0,5 моль
Шаг 6. Находим соотношение:
n(C) : n(H) : n(O) : n(Na) = 0,4 : 0,5 : 0,2 : 0,1 = 4 : 5 : 2 : 1
Простейшая формула C4H5O2Na
Однако при нагревании вещества А с NaOH образуется вещество Б, содержащее только вторичные атомы углерода и не содержащее π-связей. Это циклоалкан. Минимальный циклоалкан, в котором все атомы C вторичные — циклопропан (C3H6), но тогда в молекуле один заместитель, и условие «максимально удалены друг от друга» теряет смысл.
Следовательно, молекулярная формула удвоена: C8H10O4Na2. В молекуле два заместителя COONa и скелет C6H10 — циклогексан. Циклогексан содержит только вторичные атомы C и не содержит π-связей.
Шаг 7. Определяем структуру. Два заместителя COONa максимально удалены друг от друга в циклогексане — это положения 1 и 4.
Вещество А:
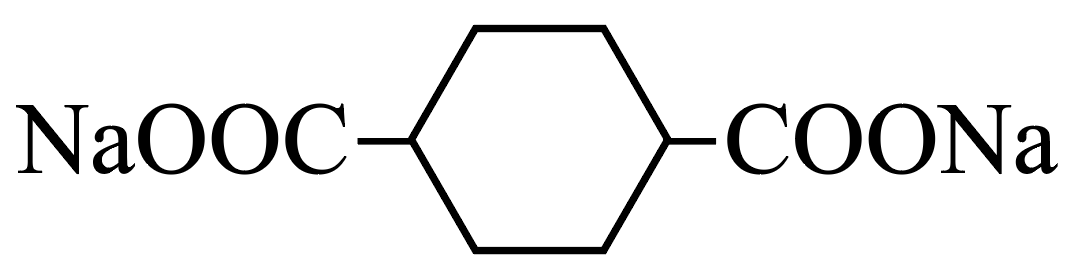
Шаг 8. При нагревании с NaOH идёт декарбоксилирование (реакция Дюма):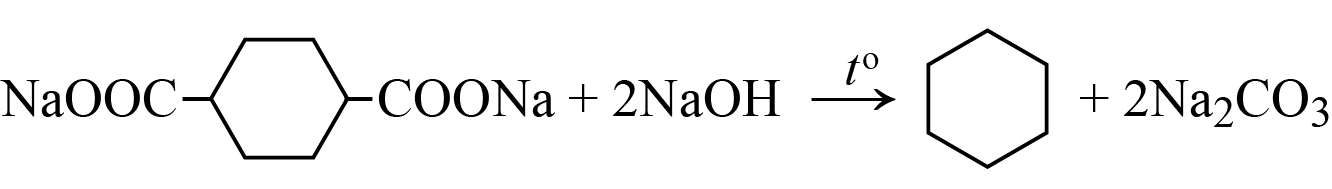
При сгорании 4,32 г органического вещества А, содержащего 66,67% углерода, было получено 2,43 г воды, 1,59 г карбоната натрия и углекислый газ. Вещество А образуется при действии раствора щелочи на вещество Б с таким же числом атомов углерода в структурной единице, три заместителя в молекуле которого расположены у нечетных атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связей атомов в его молекуле;
3) напишите уравнение реакции получения вещества А при действии раствора щелочи на вещество Б (используйте структурные формулы органических веществ).
Шаг 1. Находим массу и количество углерода в веществе А:
m(C) = 4,32 · 0,6667 = 2,88 г
n(C) = 2,88 / 12 = 0,24 моль
Шаг 2. Находим количество воды и водорода:
n(H2O) = 2,43 / 18 = 0,135 моль
n(H) = 2 · 0,135 = 0,27 моль
m(H) = 0,27 г
Шаг 3. Находим количество карбоната натрия:
n(Na2CO3) = 1,59 / 106 = 0,015 моль
Следовательно, n(Na) = 2 · 0,015 = 0,03 моль, m(Na) = 0,03 · 23 = 0,69 г
Шаг 4. Находим массу и количество кислорода по разности:
m(O) = m(A) − m(C) − m(H) − m(Na) = 4,32 − 2,88 − 0,27 − 0,69 = 0,48 г
n(O) = 0,48 / 16 = 0,03 моль
Шаг 5. Находим соотношение:
n(C) : n(H) : n(O) : n(Na) = 0,24 : 0,27 : 0,03 : 0,03 = 8 : 9 : 1 : 1
Молекулярная формула: C8H9ONa
Шаг 6. Определяем структуру. Один атом Na и один атом O — это фенолят (ArO⁻Na⁺). На органическую часть приходится C8H9. Бензольное кольцо с тремя заместителями: C6H3 + ONa + 2CH3.
Вещество Б — 3,5-диметилфенол (то же число атомов C, три заместителя у нечётных атомов углерода: OH в положении 1, CH3 в положениях 3 и 5).
Вещество А — натриевая соль 3,5-диметилфенола:
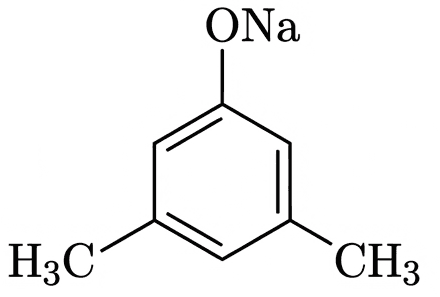
Шаг 7. Уравнение реакции:
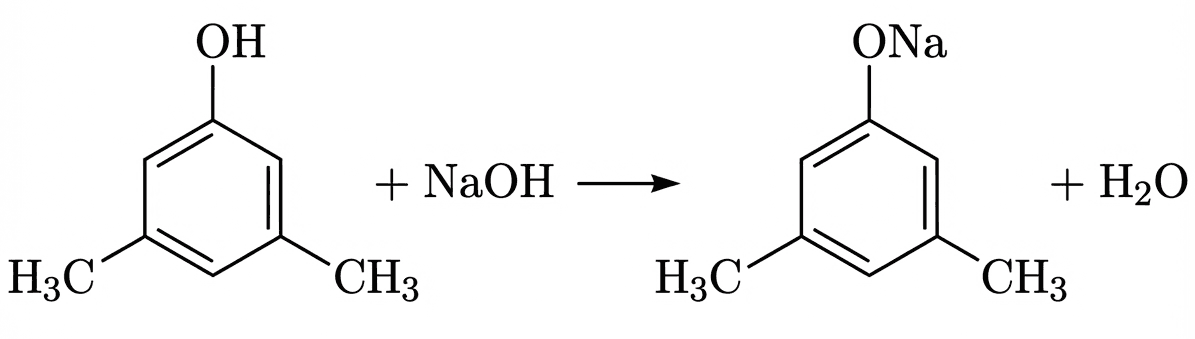
При сжигании образца органического вещества А массой 12,2 г получено 36,2 г смеси углекислого газа и воды. Молярное соотношение углекислого газа и воды в смеси составляет 7 : 3 соответственно. Данное вещество подвергается гидролизу в присутствии гидроксида натрия с образованием двух солей.
На основании данных условия задачи:
1) проведите необходимые вычисления и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение взаимодействия вещества А с гидроксидом натрия (используйте структурные формулы органических веществ).
Шаг 1. Пусть n(H2O) = x моль, тогда n(CO2) = 7x/3 моль. Составляем уравнение по массе смеси:
18x + 44 · 7x/3 = 36,2
54x/3 + 308x/3 = 36,2
362x/3 = 36,2
x = 0,3
Следовательно, n(H2O) = 0,3 моль, n(CO2) = 7 · 0,3 / 3 = 0,7 моль
Шаг 2. Находим количество углерода и водорода:
n(C) = n(CO2) = 0,7 моль
m(C) = 0,7 · 12 = 8,4 г
n(H) = 2 · n(H2O) = 2 · 0,3 = 0,6 моль
m(H) = 0,6 г
Шаг 3. Находим массу и количество кислорода по разности:
m(O) = m(A) − m(C) − m(H) = 12,2 − 8,4 − 0,6 = 3,2 г
n(O) = 3,2 / 16 = 0,2 моль
Шаг 4. Находим соотношение:
n(C) : n(H) : n(O) = 0,7 : 0,6 : 0,2 = 7 : 6 : 2
Молекулярная формула: C7H6O2
Шаг 5. Определяем структуру. Вещество гидролизуется с NaOH и даёт две соли, следовательно это сложный эфир, образованный карбоновой кислотой и фенолом.
Вещество А — фениловый эфир муравьиной кислоты:
HCOO–C6H5
Шаг 6. Уравнение реакции гидролиза:
HCOO–C6H5 + 2NaOH → HCOONa + C6H5ONa + H2O
При сгорании органического вещества А массой 11,8 г было получено 23,0 г смеси углекислого газа и воды. Молярное соотношение углекислого газа и воды в этой смеси составляет 4 : 3 соответственно. Известно, что соединение А имеет симметричное строение и реагирует с раствором гидрокарбоната калия.
На основании данных условия задачи:
1) проведите необходимые вычисления и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с избытком гидрокарбоната калия (используйте структурные формулы органических веществ).
Шаг 1. Пусть n(H2O) = x моль, тогда n(CO2) = 4x/3 моль. Составляем уравнение по массе смеси:
18x + 44 · 4x/3 = 23,0
54x/3 + 176x/3 = 23,0
230x/3 = 23,0
x = 0,3
Следовательно, n(H2O) = 0,3 моль, n(CO2) = 4 · 0,3 / 3 = 0,4 моль
Шаг 2. Находим количество углерода и водорода:
n(C) = n(CO2) = 0,4 моль
m(C) = 0,4 · 12 = 4,8 г
n(H) = 2 · n(H2O) = 2 · 0,3 = 0,6 моль
m(H) = 0,6 г
Шаг 3. Находим массу и количество кислорода по разности:
m(O) = m(A) − m(C) − m(H) = 11,8 − 4,8 − 0,6 = 6,4 г
n(O) = 6,4 / 16 = 0,4 моль
Шаг 4. Находим соотношение:
n(C) : n(H) : n(O) = 0,4 : 0,6 : 0,4 = 2 : 3 : 2
Простейшая формула C2H3O2. Вещество реагирует с KHCO3, следовательно содержит группу COOH. Строение симметричное, значит групп COOH две. Удваиваем простейшую формулу.
Молекулярная формула: C4H6O4
Шаг 5. Определяем структуру. Две группы COOH и симметричное строение — это бутандиовая кислота:
Вещество А — бутандиовая кислота:
HOOC–CH2–CH2–COOH
Шаг 6. Реакция с избытком KHCO3:
HOOC–CH2–CH2–COOH + 2KHCO3 →
→ KOOC–CH2–CH2–COOK + 2H2O + 2CO2↑
При сжигании образца органического вещества А массой 5,3 г, содержащего 45,28% кислорода, получено 13,3 г смеси углекислого газа и воды. Это вещество реагирует с натрием и со свежеосаждённым гидроксидом меди(II), молекула его содержит третичный атом углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения физических величин) и установите молекулярную формулу исходного органического вещества;
2) составьте структурную формулу исходного вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции исходного вещества с избытком натрия (используйте структурные формулы органических веществ).
Шаг 1. Находим массу и количество кислорода в веществе А:
m(O) = 5,3 · 0,4528 = 2,4 г
n(O) = 2,4 / 16 = 0,15 моль
Шаг 2. Масса углерода и водорода в веществе А:
m(C) + m(H) = m(A) − m(O) = 5,3 − 2,4 = 2,9 г
Пусть n(CO2) = x, n(H2O) = y. Составляем систему уравнений, учитывая что M(CO2) = 44 г/моль, M(H2O) = 18 г/моль:
44x + 18y = 13,3
12x + 2y = 2,9
Из второго: y = (2,9 − 12x) / 2
Подставляем в первое:
44x + 9(2,9 − 12x) = 13,3
44x + 26,1 − 108x = 13,3
−64x = −12,8
x = 0,2
y = (2,9 − 2,4) / 2 = 0,25
Следовательно, n(CO2) = 0,2 моль, n(H2O) = 0,25 моль
Шаг 3. Находим количество элементов:
n(C) = n(CO2) = 0,2 моль
n(H) = 2 · n(H2O) = 2 · 0,25 = 0,5 моль
Шаг 4. Находим соотношение:
n(C) : n(H) : n(O) = 0,2 : 0,5 : 0,15 = 4 : 10 : 3
Молекулярная формула: C4H10O3
Шаг 5. Определяем структуру. Вещество реагирует с натрием — содержит OH-группы. Реагирует со свежеосаждённым Cu(OH)2 — многоатомный спирт с OH на соседних атомах C. Три атома O — три группы OH. Третичный атом углерода.
Вещество А — 2-метилпропантриол-1,2,3:
Шаг 6. Реакция с избытком натрия:
При сгорании органического вещества A массой 0,8 г, содержащего 32% кислорода по массе, получено 896 мл (н.у.) углекислого газа и некоторое количество воды. Известно, что вещество A вступает в реакцию с раствором гидроксида бария при нагревании, в результате чего образуется предельный одноатомный спирт и соль, кислотный остаток которой содержит три атома углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества A;
2) составьте возможную структурную формулу вещества A, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества A с раствором гидроксида бария при нагревании (используйте структурные формулы органических веществ).
Шаг 1. Находим количество CO2:
V(CO2) = 896 мл = 0,896 л
n(CO2) = 0,896 / 22,4 = 0,04 моль
n(C) = n(CO2) = 0,04 моль
m(C) = 0,04 · 12 = 0,48 г
Шаг 2. Находим массу и количество кислорода в веществе А:
m(O) = 0,8 · 0,32 = 0,256 г
n(O) = 0,256 / 16 = 0,016 моль
Шаг 3. Находим массу и количество водорода по разности:
m(H) = m(A) − m(C) − m(O) = 0,8 − 0,48 − 0,256 = 0,064 г
n(H) = 0,064 / 1 = 0,064 моль
Шаг 4. Находим соотношение:
n(C) : n(H) : n(O) = 0,04 : 0,064 : 0,016 = 5 : 8 : 2
Молекулярная формула: C5H8O2
Шаг 5. Определяем структуру. Вещество реагирует с Ba(OH)2 при нагревании — это гидролиз сложного эфира. Продукты: предельный одноатомный спирт и соль, кислотный остаток которой содержит 3 атома C.
На спиртовую часть остаётся 5 − 3 = 2 атома C — это этанол C2H5OH (предельный, одноатомный).
Кислотный остаток с 3 атомами C: если кислота предельная (пропановая), эфир C5H10O2 — не совпадает с формулой. Следовательно, кислота непредельная — пропеновая CH2=CH–COOH. Эфир CH2=CH–COOC2H5 = C5H8O2 ✓
Вещество А — этиловый эфир пропеновой кислоты:
CH2=CH–COOC2H5
Шаг 6. Уравнение гидролиза с Ba(OH)2:
2CH2=CH–COOC2H5 + Ba(OH)2 → (CH2=CH–COO)2Ba + 2C2H5OH
При сгорании 40,95 г органического вещества, содержащего 11,97% азота по массе получили 39,2 л углекислого газа (н.у.), 34,65 г воды и некоторое количество азота. При нагревании с соляной кислотой данное вещество подвергается гидролизу, продуктами которого являются соединение состава C2H6NO2Cl и вторичный спирт.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу органического вещества;
2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции гидролиза исходного вещества в присутствии соляной кислоты (используйте структурные формулы органических веществ).
Шаг 1. Находим количество CO2 и углерода:
n(CO2) = 39,2 / 22,4 = 1,75 моль
n(C) = n(CO2) = 1,75 моль
m(C) = 1,75 · 12 = 21 г
Шаг 2. Находим количество воды и водорода:
n(H2O) = 34,65 / 18 = 1,925 моль
n(H) = 2 · 1,925 = 3,85 моль
m(H) = 3,85 г
Шаг 3. Находим массу и количество азота:
m(N) = 40,95 · 0,1197 = 4,9 г
n(N) = 4,9 / 14 = 0,35 моль
Шаг 4. Находим массу и количество кислорода по разности:
m(O) = m(A) − m(C) − m(H) − m(N) = 40,95 − 21 − 3,85 − 4,9 = 11,2 г
n(O) = 11,2 / 16 = 0,7 моль
Шаг 5. Находим соотношение:
n(C) : n(H) : n(O) : n(N) = 1,75 : 3,85 : 0,7 : 0,35 = 5 : 11 : 2 : 1
Молекулярная формула: C5H11NO2
Шаг 6. Определяем структуру. При гидролизе с HCl образуется C2H6NO2Cl — это гидрохлорид аминоуксусной кислоты (ClH3N–CH2–COOH). Второй продукт — вторичный спирт.
Из C5H11NO2 вычитаем фрагмент аминоуксусной кислоты (NH2–CH2–COO = C2H4NO2), остаётся C3H7 — изопропильная группа (вторичный спирт = пропанол-2).
Вещество А — изопропиловый эфир аминоуксусной кислоты:
Шаг 7. Уравнение гидролиза:
Вещество А состава CxH2x+3NyO2y содержит 30,48% кислорода по массе. При сгорании 42 г вещества А образуется 35,84 л (н.у.) углекислого газа, вода и азот. Известно, что вещество А взаимодействует с водным раствором гидроксида калия при нагревании, при этом образуются два продукта, содержащие одинаковое количество атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте одну из возможных структурных формул вещества А, которая отражает порядок связи атомов в его формульной единице;
3) напишите уравнение реакции вещества А с водным раствором гидроксида калия при нагревании (используйте структурные формулы органических веществ).
Шаг 1. Находим количество CO2 и углерода:
n(CO2) = 35,84 / 22,4 = 1,6 моль
n(C) = n(CO2) = 1,6 моль
m(C) = 1,6 · 12 = 19,2 г
Шаг 2. Из общей формулы CxH2x+3NyO2y выразим массовую долю кислорода:
ω(O) = 32y / M(A) = 0,3048
Шаг 3. Найдём M(A). Из формулы: n(C) = x · n(A), следовательно, n(A) = 1,6 / x
M(A) = m(A) / n(A) = 42 / (1,6 / x) = 42x / 1,6 = 26,25x
Шаг 4. Подставляем в выражение для массовой доли кислорода:
32y / 26,25x = 0,3048
32y = 8x
y = x/4
Шаг 5. Также M(A) = 12x + 2x + 3 + 14y + 32y = 14x + 3 + 46y
Подставляем y = x/4:
M(A) = 14x + 3 + 46x/4 = 14x + 3 + 11,5x = 25,5x + 3
Приравниваем к 26,25x:
26,25x = 25,5x + 3
0,75x = 3
x = 4, y = 1
Молекулярная формула: C4H11NO2
Шаг 6. Определяем структуру. Вещество реагирует с KOH при нагревании, даёт два продукта с одинаковым числом атомов C. Всего 4 атома C, следовательно, каждый продукт содержит по 2 атома C.
C4H11NO2 — ионное соединение, в котором катион содержит азот, а анион — карбоксилатную группу. Оба продукта реакции с KOH содержат по 2 атома C, следовательно, кислотный остаток — ацетат, а катион — этиламмоний.
Вещество А — ацетат этиламмония:
[C2H5NH3]+[CH3COO]−
Шаг 7. Уравнение реакции:
[C2H5NH3]+[CH3COO]− + KOH → CH3COOK + C2H5NH2 + H2O
Вещество A состава CxHxNyO2y содержит 14,88% кислорода по массе. Известно, что 21,5 г вещества A реагируют с раствором, содержащим 8,55 г гидроксида бария, причём эти вещества взаимодействуют в молярном соотношении 2:1.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте одну из возможных структурных формул вещества А, которая отражает порядок связи атомов в его формульной единице;
3) напишите уравнение реакции вещества А с водным раствором гидроксида бария при нагревании (используйте структурные формулы органических веществ).
Шаг 1. Находим количество Ba(OH)2:
n(Ba(OH)2) = 8,55 / 171 = 0,05 моль
Шаг 2. Из соотношения 2:1:
n(A) = 2 · 0,05 = 0,1 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 21,5 / 0,1 = 215 г/моль
Шаг 4. Находим y из массовой доли кислорода. Формула CxHxNyO2y:
ω(O) = 32y / 215 = 0,1488
32y = 32
y = 1
Следовательно, в молекуле 1 атом азота и 2 атома кислорода.
Шаг 5. Находим x:
M(A) = 12x + x + 14 + 32 = 215
13x + 46 = 215
13x = 169
x = 13
Молекулярная формула: C13H13NO2
Шаг 6. Определяем структуру. Вещество реагирует с Ba(OH)2 в соотношении 2:1 — ионное соединение, в котором катион содержит азот, а анион — карбоксилатную группу. Два атома O — одна группа COO⁻. Один атом N — в составе катиона.
13 атомов C распределяем: 7 атомов C на анион (бензоат C6H5COO⁻) и 6 атомов C на катион (фениламмоний C6H5NH3⁺).
Вещество А — бензоат фениламмония:
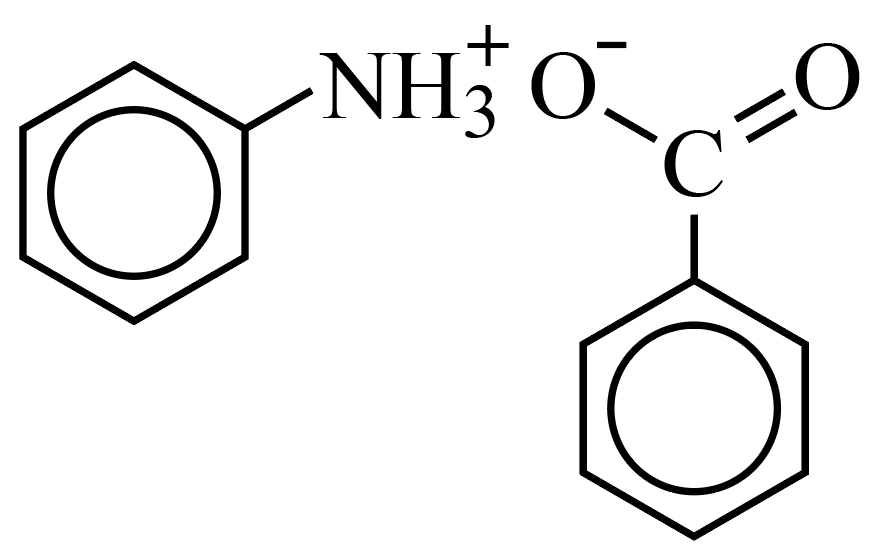
Шаг 7. Уравнение реакции:
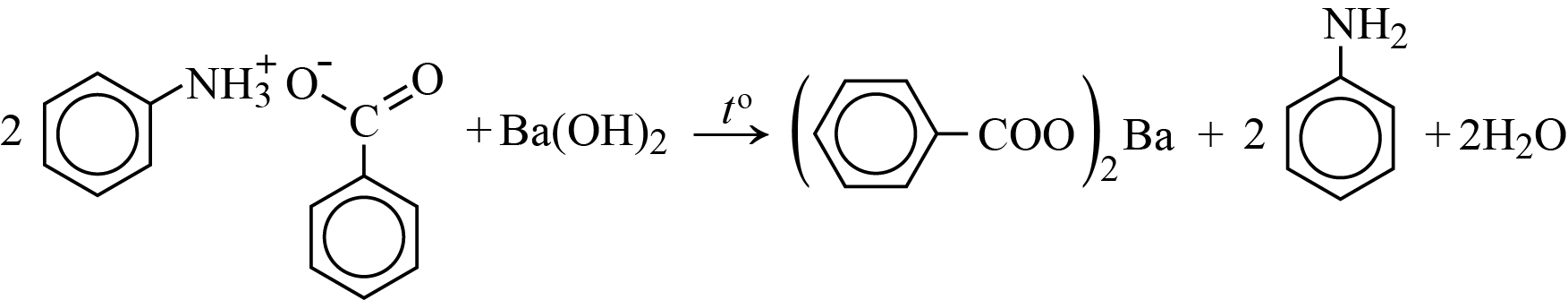
Вещество А содержит по массе 18,90% углерода, 11,02% азота, 25,20% серы, 37,80% кислорода и водород. Вещество А образуется при пропускании избытка сернистого газа через водный раствор вещества Б.
На основании данных условия задачи:
1) проведите необходимые вычисления и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая отражает порядок связей атомов в его молекуле;
3) напишите уравнение реакции получения вещества А при взаимодействии вещества Б с сернистым газом в воде (используйте структурные формулы органических веществ).
Шаг 1. Находим массовую долю водорода:
ω(H) = 100% − 18,90% − 11,02% − 25,20% − 37,80% = 7,08%
Шаг 2. Берём образец 100 г и находим количества элементов:
n(C) = 18,90 / 12 = 1,575 моль
n(N) = 11,02 / 14 = 0,787 моль
n(S) = 25,20 / 32 = 0,7875 моль
n(O) = 37,80 / 16 = 2,3625 моль
n(H) = 7,08 / 1 = 7,08 моль
Шаг 3. Находим соотношение, делим на наименьшее (0,787):
n(C) : n(N) : n(S) : n(O) : n(H) = 1,575 : 0,787 : 0,7875 : 2,3625 : 7,08 = 2 : 1 : 1 : 3 : 9
Молекулярная формула: C2H9NO3S
Шаг 4. Определяем структуру. Вещество образуется при пропускании избытка SO2 через водный раствор вещества Б. SO2 в воде даёт сернистую кислоту H2SO3. При избытке SO2 образуется кислая соль — гидросульфит.
Вещество Б — азотсодержащее органическое вещество, которое реагирует с сернистой кислотой. Это амин. С 2 атомами C — этиламин C2H5NH2.
Вещество А — гидросульфит этиламмония:
[C2H5NH3]+[HSO3]−
Шаг 5. Уравнение реакции:
C2H5NH2 + H2O + SO2 →
→ [C2H5NH3]+[HSO3]−
Вещество А состава CxH10+xBryNy содержит 57,97 % брома по массе. Известно, что 6,90 г вещества А можно получить при взаимодействии азотсодержащего органического вещества Б с раствором, содержащим 4,05 г бромоводорода, причём эти вещества взаимодействуют в молярном соотношении 1:2.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим количество HBr:
n(HBr) = 4,05 / 81 = 0,05 моль
Шаг 2. Из соотношения 1:2:
n(Б) = 0,05 / 2 = 0,025 моль
n(A) = n(Б) = 0,025 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 6,90 / 0,025 = 276 г/моль
Шаг 4. Находим y из массовой доли брома. Формула CxH10+xBryNy:
ω(Br) = 80y / 276 = 0,5797
80y = 160
y = 2
Следовательно, в молекуле 2 атома Br и 2 атома N.
Шаг 5. Находим x:
M(A) = 12x + 10 + x + 160 + 28 = 276
13x + 198 = 276
13x = 78
x = 6
Молекулярная формула: C6H16Br2N2
Шаг 6. Определяем структуру. Вещество Б — азотсодержащее, реагирует с HBr в соотношении 1:2, следовательно, Б — диамин с двумя группами NH2. Вещество А — его соль с HBr.
Из C6H16Br2N2 убираем 2HBr, получаем вещество Б: C6H14N2. Степень ненасыщенности = (12 + 2 − 14 + 2) / 2 = 1, следовательно, в молекуле один цикл. Это циклогексан с двумя группами NH2 — 1,4-диаминоциклогексан.
Вещество Б: H2N–C6H10–NH2 (1,4-диаминоциклогексан)
Вещество А:
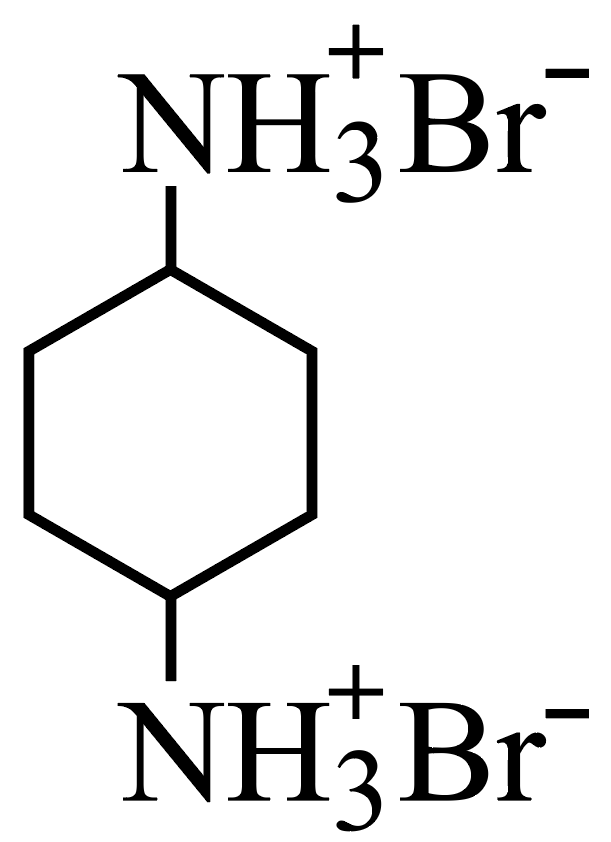
Шаг 7. Уравнение реакции:
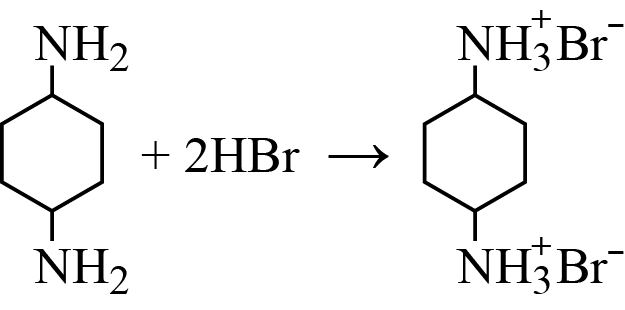
Вещество А состава CxH2x+6N2yO3y содержит 26,67% кислорода по массе и не содержит углерод-углеродных связей. Известно, что 18,0 г вещества А реагируют с раствором, содержащим 17,1 г гидроксида бария, причём эти вещества взаимодействуют в молярном соотношении 1:1, а одним из продуктов реакции является осадок.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с гидроксидом бария (используйте структурные формулы органических веществ).
Шаг 1. Находим количество Ba(OH)2:
n(Ba(OH)2) = 17,1 / 171 = 0,1 моль
Шаг 2. Из соотношения 1:1:
n(A) = 0,1 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 18,0 / 0,1 = 180 г/моль
Шаг 4. Находим y из массовой доли кислорода. Формула CxH2x+6N2yO3y:
ω(O) = 48y / 180 = 0,2667
48y = 48
y = 1
Следовательно, в молекуле 2 атома N и 3 атома O.
Шаг 5. Находим x:
M(A) = 12x + 2x + 6 + 28 + 48 = 180
14x + 82 = 180
14x = 98
x = 7
Молекулярная формула: C7H20N2O3
Шаг 6. Определяем структуру. Вещество реагирует с Ba(OH)2, одним из продуктов является осадок — это BaCO3, следовательно, в веществе А присутствует карбонат-ион CO32−. Два атома N — два катиона, содержащие азот.
Из C7H20N2O3 вычитаем фрагмент CO3 (1C, 3O), остаётся C6H20N2 — два одинаковых катиона, следовательно, каждый содержит C3H10N. Вещество не содержит C–C связей, значит к азоту присоединены только метильные группы — это катион триметиламмония (CH3)3NH+.
Вещество А — карбонат триметиламмония: [(CH3)3NH]2CO3
Шаг 7. Уравнение реакции:
[(CH3)3NH]2CO3 + Ba(OH)2 → BaCO3↓ + 2 (CH3)3N + 2 H2O
Вещество А состава CxHx+1NyO2yNay содержит 17,11% кислорода по массе. Известно, что 18,7 г вещества А можно получить при взаимодействии кислородсодержащего органического вещества Б с раствором, содержащим 4,0 г гидроксида натрия, причём эти вещества взаимодействуют в молярном соотношении 1:1. В молекуле вещества Б азотсодержащая функциональная группа находится в α-положении по отношению к кислородсодержащей функциональной группе, а в ароматическом кольце замещён только один атом водорода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим количество NaOH:
n(NaOH) = 4,0 / 40 = 0,1 моль
Шаг 2. Из соотношения 1:1:
n(Б) = 0,1 моль
n(A) = n(Б) = 0,1 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 18,7 / 0,1 = 187 г/моль
Шаг 4. Находим y из массовой доли кислорода. Формула CxHx+1NyO2yNay:
ω(O) = 32y / 187 = 0,1711
32y = 32
y = 1
Следовательно, в молекуле 1 атом N, 2 атома O и 1 атом Na.
Шаг 5. Находим x:
M(A) = 12x + x + 1 + 14 + 32 + 23 = 187
13x + 70 = 187
13x = 117
x = 9
Молекулярная формула: C9H10NO2Na
Шаг 6. Определяем структуру. Вещество А содержит Na и образуется из вещества Б при взаимодействии с NaOH в соотношении 1:1, следовательно, вещество Б содержит одну кислотную группу — COOH. Азотсодержащая группа (NH2) находится в α-положении к кислородсодержащей (COOH), следовательно, вещество Б — α-аминокислота.
Из C9H10NO2Na вычитаем фрагмент COONa и NH2, на углеводородный скелет остаётся C7H7. В ароматическом кольце замещён только один атом водорода, следовательно, C7H7 = C6H5–CH2 (бензильная группа).
Вещество Б — 2-амино-3-фенилпропановая кислота: C6H5–CH2–CH(NH2)–COOH
Вещество А — натриевая соль 2-амино-3-фенилпропановой кислоты: C6H5–CH2–CH(NH2)–COONa
Шаг 7. Уравнение реакции:
C6H5–CH2–CH(NH2)–COOH + NaOH → C6H5–CH2–CH(NH2)–COONa + H2O
Вещество А состава CxH2yO2yNay содержит 45,71% углерода по массе. Известно, что 10,5 г вещества А можно получить при взаимодействии кислородсодержащего органического вещества Б с раствором, содержащим 4,0 г гидроксида натрия, причём эти вещества взаимодействуют в молярном соотношении 1:2. Известно, что функциональные группы в веществе А и максимально удалены друг от друга. При нагревании вещества А с гидроксидом натрия образуется вещество, которое не обесцвечивает бромную воду.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с гидроксидом натрия с получением вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим количество NaOH:
n(NaOH) = 4,0 / 40 = 0,1 моль
Шаг 2. Из соотношения 1:2:
n(Б) = 0,1 / 2 = 0,05 моль
n(A) = n(Б) = 0,05 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 10,5 / 0,05 = 210 г/моль
Шаг 4. Находим x из массовой доли углерода. Формула CxH2yO2yNay:
ω(C) = 12x / 210 = 0,4571
12x = 96
x = 8
Шаг 5. Находим y:
M(A) = 96 + 2y + 32y + 23y = 96 + 57y = 210
57y = 114
y = 2
Молекулярная формула: C8H4O4Na2
Шаг 6. Определяем структуру. Два атома Na и четыре атома O — две группы COONa. Функциональные группы максимально удалены друг от друга — пара-положение в бензольном кольце. При нагревании с NaOH образуется вещество Б, которое не обесцвечивает бромную воду — это бензол (реакция декарбоксилирования).
Вещество А — терефталат натрия:
Шаг 7. Уравнение реакции (декарбоксилирование):
Вещество А состава CxH2x+6N2yO3y содержит 48,0% кислорода по массе. Известно, что 10,0 г вещества А можно получить при взаимодействии азотсодержащего органического вещества Б с раствором, содержащим 6,3 г азотной кислоты, причём эти вещества взаимодействуют в молярном соотношении 1:2. В молекуле вещества Б азотсодержащие функциональные группы расположены у соседних атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим количество HNO3:
n(HNO3) = 6,3 / 63 = 0,1 моль
Шаг 2. Из соотношения 1:2:
n(Б) = 0,1 / 2 = 0,05 моль
n(A) = n(Б) = 0,05 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 10,0 / 0,05 = 200 г/моль
Шаг 4. Находим y из массовой доли кислорода. Формула CxH2x+6N2yO3y:
ω(O) = 48y / 200 = 0,48
48y = 96
y = 2
Следовательно, в молекуле 4 атома N и 6 атомов O.
Шаг 5. Находим x:
M(A) = 14x + 6 + 76y = 14x + 6 + 152 = 200
14x = 42
x = 3
Молекулярная формула: C3H12N4O6
Шаг 6. Определяем структуру. Вещество Б — азотсодержащее органическое вещество, реагирует с HNO3 в соотношении 1:2, следовательно, Б — диамин с двумя группами NH2. Вещество А — его соль с азотной кислотой (динитрат).
Из C3H12N4O6 вычитаем 2 HNO3, получаем вещество Б: C3H10N2. Азотсодержащие группы расположены у соседних атомов углерода — это 1,2-диаминопропан.
Вещество Б — 1,2-диаминопропан: CH3–CH(NH2)–CH2–NH2
Вещество А:
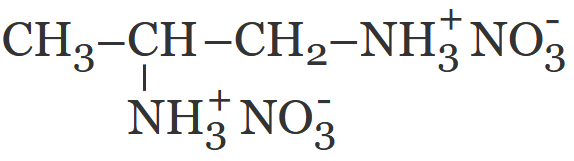
Шаг 7. Уравнение реакции:
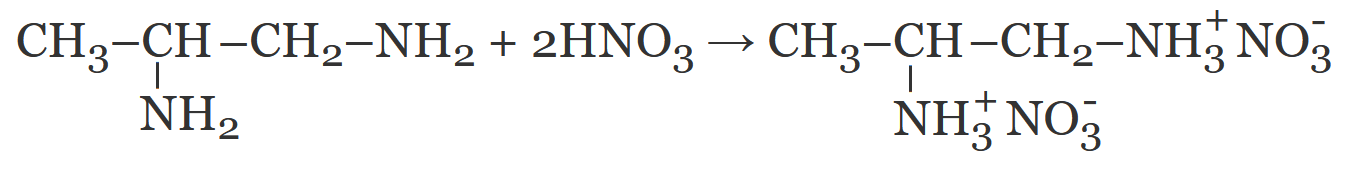
Вещество А состава CxH2xNyO3y содержит 63,16% кислорода по массе. Известно, что 7,6 г вещества А можно получить при взаимодействии кислородсодержащего органического вещества Б с раствором, содержащим 6,3 г азотной кислоты, причём эти вещества взаимодействуют в молярном соотношении 1:2. Вещество Б реагирует со свежеосаждённым гидроксидом меди(II) при комнатной температуре.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции получения вещества А из вещества Б (используйте структурные формулы органических веществ).
Шаг 1. Находим количество HNO3:
n(HNO3) = 6,3 / 63 = 0,1 моль
Шаг 2. Из соотношения 1:2:
n(Б) = 0,1 / 2 = 0,05 моль
n(A) = n(Б) = 0,05 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 7,6 / 0,05 = 152 г/моль
Шаг 4. Находим y из массовой доли кислорода. Формула CxH2xNyO3y:
ω(O) = 48y / 152 = 0,6316
48y = 96
y = 2
Следовательно, в молекуле 2 атома N и 6 атомов O.
Шаг 5. Находим x:
M(A) = 14x + 62y = 14x + 124 = 152
14x = 28
x = 2
Молекулярная формула: C2H4N2O6
Шаг 6. Определяем структуру. Вещество Б — кислородсодержащее органическое вещество, реагирует с HNO3 в соотношении 1:2 и со свежеосаждённым Cu(OH)2 при комнатной температуре, следовательно, Б — многоатомный спирт с OH-группами на соседних атомах C.
Из C2H4N2O6 вычитаем 2 фрагмента NO3, получаем вещество Б: C2H4(OH)2 — этиленгликоль.
Вещество Б — этиленгликоль: HO–CH2–CH2–OH
Вещество А — динитрат этиленгликоля: O2N–O–CH2–CH2–O–NO2
Шаг 7. Уравнение реакции:
HO–CH2–CH2–OH + 2HNO3 → O2N–O–CH2–CH2–O–NO2 + 2H2O
Вещество А состава CxHyNyO2y+1 содержит 48,91% кислорода по массе. Известно, что 22,9 г вещества А реагируют с раствором, содержащим 4,0 г гидроксида натрия, причём эти вещества взаимодействуют в молярном соотношении 1:1. В молекуле вещества А функциональные группы расположены в положениях 1, 2, 4 и 6.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с гидроксидом натрия (используйте структурные формулы органических веществ).
Шаг 1. Находим количество NaOH:
n(NaOH) = 4,0 / 40 = 0,1 моль
Шаг 2. Из соотношения 1:1:
n(A) = 0,1 моль
Шаг 3. Находим молярную массу вещества А:
M(A) = 22,9 / 0,1 = 229 г/моль
Шаг 4. Находим y из массовой доли кислорода. Формула CxHyNyO2y+1:
ω(O) = 16(2y+1) / 229 = 0,4891
32y + 16 = 112
32y = 96
y = 3
Следовательно, в молекуле 3 атома H, 3 атома N и 7 атомов O.
Шаг 5. Находим x:
M(A) = 12x + 47y + 16 = 12x + 157 = 229
12x = 72
x = 6
Молекулярная формула: C6H3N3O7
Шаг 6. Определяем структуру. Вещество реагирует с NaOH в соотношении 1:1, следовательно, содержит одну кислотную группу. Формула C6H3N3O7 с высокой степенью ненасыщенности указывает на ароматическое кольцо. Один кислород приходится на OH-группу (фенольную), остальные шесть — на три нитрогруппы NO2. Функциональные группы в положениях 1, 2, 4 и 6: OH в положении 1, NO2 в положениях 2, 4 и 6.
Вещество А — 2,4,6-тринитрофенол:
Шаг 7. Уравнение реакции:

отлично
Cпасибо за ваш труд
Большое спасибо за помощь нам, учителям
очень рад, что сделал, действительно, что-то полезное
Здравствуйте! Спасибо за чудесный материал! Уточните, пожалуйста, в задаче 14 степень ненасыщенности в C6H14N2= (12+2-14+2)/2. Это выражение как получилось?
Формула степени ненасыщенности (она же индекс водородной недостаточности) для соединения CₙHₘNₖ:
DBE = (2n + 2 − m + k) / 2
Азот прибавляется, потому что каждый атом азота «приносит» одну дополнительную связь по сравнению с углеродом (валентность 3 вместо 2 у кислорода или 1 у водорода). Можно запомнить так: азот считается как «полуглерод» — он увеличивает максимально возможное число водородов на 1.
Для C₆H₁₄N₂:
DBE = (2·6 + 2 − 14 + 2) / 2 = (12 + 2 − 14 + 2) / 2 = 2/2 = 1
Одна степень ненасыщенности = один цикл или одна двойная связь. Раз в задаче предполагается насыщенное соединение (диамин), значит это цикл.
Спасибо за своевременные прекрасные задачи! Благодарю от имени учителей и учеников!
11 задача. 42x/1,6=26,25х
Мы не можем разделить на 1,6, так как в знаменателе нет х. Здесь опечатка?
нет, все математически верно.
Спасибо за прекрасную и своевременную работу!!!
Здравствуйте! Подскажите пожалуйста, во второй задаче может быть метилпропандиовая кислота?
Здравствуйте! Да, метилпропандиовая кислота полностью удовлетворяет условию задачи — молекулярная формула соли та же (C₄H₄O₄K₂), все расчёты сходятся. На экзамене такое альтернативное решение должно быть засчитано.
Здравствуйте, в условии 9 задачи сказано, что в продуктах получается одноатомный спирт и соль с кислотным остатком, содержащим 3 атома углерода, но по молекулярной формуле и решению получается этанол.. Если все верно, можете, пожалуйста, объяснить, как к этому пришли через метанол в условии?
Здравствуйте! В условии нет упоминания метанола. Решение: молекулярная формула C₅H₈O₂. Кислотный остаток с 3 атомами C — это пропеноат (CH₂=CH-COO⁻). На спирт остаётся 2 атома C — это этанол C₂H₅OH. Вещество А — этиловый эфир пропеновой кислоты CH₂=CH-COO-C₂H₅ (этилакрилат). Спирт — именно этанол, всё верно.
Задача 17.
У вас вещество Б — это одновременно и терефталевая кислота (прекурсор вещества А) и бензол, продукт реакции.
К слову, а нельзя ли было найти переменную y проще?
Исходя из того, что кислородсодержащее вещество Б реагирует с двумя молекулами гидроксида, мы автоматически имеем y = 2. Или мы не могли исходить из предположения, что вещество Б само не содержало атомов натрия, и должны были доказать это уравнением?
Здравствуйте. Да, действительно, можно. Такая же ситуация и с заданиями от ФИПИ, которые они дали в качестве привера. Я бы делал так — расчитал строго математически значение у, а данные о соотношение при взаимодействии использовал как дополнительную проверку соответствия условию.
Второе замечание по делу, чуть скорректировал условие.
Ошибка в задаче 17: по условию веществом Б является одновременно телефталевая кислота и бензол.
спасибо, условие скорректировал
