



Мы уже знаем, что атомы химических элементов могут отличаться друг от друга по составу и, очевидно, что это должно влиять на их массу, поскольку чем больше в ядре атома суммарное количество протонов и нейтронов, тем он тяжелее. Электроны практически не влияют на массу атома, поскольку обладают крайне малой по сравнению с нейтронами и протонами массой (mp/me~2000).
Так как количество протонов в каждом атоме всегда равно количеству электронов, а электроны, если рассматривать строение атома упрощенно, движутся вокруг ядра на значительном от него удалении, то радиус атома равен радиусу орбиты наиболее удаленного от ядра электрона. Следовательно, должна быть некоторая зависимость радиуса атома от количества таких орбит, которая в какой-то степени связана с количеством электронов.
Среди химических элементов наименьшие размеры имеют атомы водорода, радиус которых в обычном состоянии составляет всего лишь около 0,0000000000529 м (5,2910-11 м) или 0,529 Å, где Å – обозначение единицы длины, называемой ангстрем и равной 10-10 м. Кроме того, в качестве единиц измерения таких малых значений расстояний часто используют нанометры (нм). 1 нанометр равен 10-9 м.
Легко догадаться, что малы не только размеры всех атомов, но и их массы. Так, например, масса атома водорода приблизительно равна 1,674∙10-27 кг. Масса атома, выражаемая в килограммах (г, мг и т.д.), называется абсолютной атомной массой и обозначается как ma. Проводить расчеты с такими малыми величинами крайне неудобно, поэтому ученые нашли следующий выход – измерять все массы атомов других химических элементов в «атомах водорода». Таким образом, получалось, что, например, атом кислорода весит приблизительно 16 «атомов водорода», атом углерода — «12 атомов водорода» и т.д. И все бы хорошо, но все испортили изотопы – разновидности атомов одного и того же химического элемента, отличающиеся между собой массой из-за разного количества нейтронов в ядрах. Выходом могло бы стать использование некой средней массы атома водорода, но дело осложняется тем, что разные изотопы водорода в природе распространены неравномерно. Поэтому, в конечном итоге, было решено использовать в качестве относительной единицы массы не массу атома водорода, а одну двенадцатую массы атома углерода, поскольку данный элемент представлен практически полностью только изотопами углерода с 6 нейтронами и 6 протонами в ядрах (~99 %). Одну двенадцатую массы атома данного изотопа углерода было принято обозначать 1 а.е.м., что расшифровывается как «атомная единица массы». Одна атомная единица массы равно примерно 1,66·10−27 кг.
Графическое представление смысла одной атомной единицы массы представлено на рисунке 2.
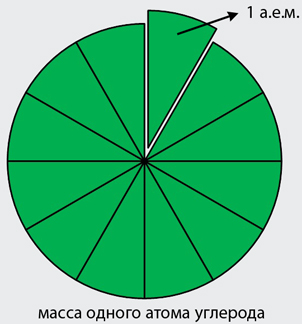
Таким образом, мы подошли к определению нового термина – относительной атомной массы:
Определение: относительная атомная масса химического элемента равна отношению его абсолютной массы к одной двенадцатой абсолютной массы атома углерода или к массе одной атомной единицы массы.
Относительную атомную массу обозначают символом Ar (индекс r означает сокращение от английского слова relative, что переводится как «относительный»). Таким образом, обозначив в общем виде химический элемент символом Х, мы получаем следующую формульную запись представленного выше определения:
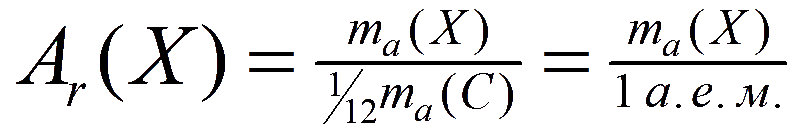
Относительная атомная масса — величина безразмерная, так как в числителе и знаменателе находятся значения, измеряемые в одинаковых единицах массы (кг, г или др.). Согласно представленной выше формуле, например, относительная атомная масса водорода равна:
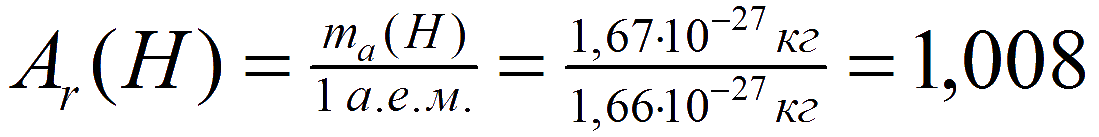
а относительная атомная масса кислорода:
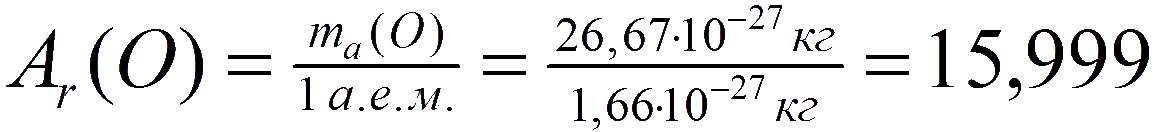
В большинстве расчетных задач, с которыми приходится иметь дело химикам, используются значения относительных атомных масс, округленные до целочисленных значений, т.е. применительно к водороду и кислороду:
![]()
Следует отметить, что атомную массу хлора округляют до 35,5. Это связано с тем, что у данного элемента наиболее распространенные в природе изотопы имеют относительные атомные массы 35 и 37, а их содержание в смеси близко к 3:1 в пользу более легкого.

Природный хлор состоит из двух стабильных изотопов: 35Cl (75,53 %), 37Cl (24,47 %).
Добрый день! Замечание справедливое, сейчас исправлю. Благодарю за бдительность!
