



Крайне редко химические вещества состоят из отдельных, не связанных между собой атомов химических элементов. Таким строением в обычных условиях обладает лишь небольшой ряд газов называемых благородными: гелий, неон, аргон, криптон, ксенон и радон. Чаще же всего химические вещества состоят не из разрозненных атомов, а из их объединений в различные группировки. Такие объединения атомов могут насчитывать несколько единиц, сотен, тысяч или даже больше атомов. Сила, которая удерживает эти атомы в составе таких группировок, называется химическая связь.
Другими словами, можно сказать, что химической связью называют взаимодействие, которое обеспечивает связь отдельных атомов в более сложные структуры (молекулы, ионы, радикалы, кристаллы и др.).
Причиной образования химической связи является то, что энергия более сложных структур меньше суммарной энергии отдельных, образующих ее атомов.
Так, в частности, если при взаимодействии атомов X и Y образуется молекула XY, это означает, что внутренняя энергия молекул этого вещества ниже, чем внутренняя энергия отдельных атомов, из которых оно образовалось:
E(XY) < E(X) + E(Y)
По этой причине при образовании химических связей между отдельными атомами выделятся энергия.
Упрощенно можно считать, что в основе химических связей лежат электростатические силы, обусловленные взаимодействиями положительно заряженных ядер и отрицательно заряженных электронов.
В образовании химических связей элементов главных подгрупп принимают участие электроны внешнего электронного слоя с наименьшей энергией связи с ядром, называемые валентными. Например, у бора таковыми являются электроны 2 энергетического уровня – 2 электрона на 2s-орбитали и 1 на 2p-орбитали:
При образовании химической связи каждый атом стремится получить электронную конфигурацию атомов благородных газов, т.е. чтобы в его внешнем электронном слое было 8 электронов (2 для элементов первого периода). Это явление получило название правила октета.
Достижение атомами электронной конфигурации благородного газа возможно, если изначально одиночные атомы сделают часть своих валентных электронов общими для других атомов. При этом образуются общие электронные пары.
В зависимости от степени обобществления электронов можно выделить ковалентную, ионную и металлическую связи.
Ковалентная связь возникает чаще всего между атомами элементов неметаллов. Если атомы неметаллов, образующие ковалентную связь, относятся к разным химическим элементам, такую связь называют ковалентной полярной. Причина такого названия кроется в том, что атомы разных элементов имеют и различную способность притягивать к себе общую электронную пару. Очевидно, что это приводит к смещению общей электронной пары в сторону одного из атомов, в результате чего на нем формируется частичный отрицательный заряд. В свою очередь, на другом атоме формируется частичный положительный заряд. Например, в молекуле хлороводорода электронная пара смещена от атома водорода к атому хлора:
Примеры веществ с ковалентной полярной связью:
СCl4, H2S, CO2, NH3, SiO2 и т.д.
Ковалентная неполярная связь образуется между атомами неметаллов одного химического элемента. Поскольку атомы идентичны, одинакова и их способность оттягивать на себя общие электроны. В связи с этим смещения электронной пары не наблюдается:
Вышеописанный механизм образования ковалентной связи, когда оба атома предоставляют электроны для образования общих электронных пар, называется обменным.
Также существует и донорно-акцепторный механизм.
При образовании ковалентной связи по донорно-акцепторному механизму общая электронная пара образуется за счет заполненной орбитали одного атома (с двумя электронами) и пустой орбитали другого атома. Атом, предоставляющий неподеленную электронную пару, называют донором, а атом со свободной орбиталью – акцептором. В качестве доноров электронных пар выступают атомы, имеющие спаренные электроны, например N, O, P, S.
Например, по донорно-акцепторному механизму происходит образование четвертой ковалентной связи N-H в катионе аммония NH4+:
Помимо полярности ковалентные связи также характеризуются энергией. Энергией связи называют минимальную энергию, необходимую для разрыва связи между атомами.
Энергия связи уменьшается с ростом радиусов связываемых атомов. Так, как мы знаем, атомные радиусы увеличиваются вниз по подгруппам, можно, например, сделать вывод о том, что прочность связи галоген-водород увеличивается в ряду:
HI < HBr < HCl < HF
Также энергия связи зависит от ее кратности – чем больше кратность связи, тем больше ее энергия. Под кратностью связи понимается количество общих электронных пар между двумя атомами.
Ионную связь можно рассматривать как предельный случай ковалентной полярной связи. Если в ковалентной-полярной связи общая электронная пара смещена частично к одному из пары атомов, то в ионной она практически полностью «отдана» одному из атомов. Атом, отдавший электрон(ы), приобретает положительный заряд и становится катионом, а атом, забравший у него электроны, приобретает отрицательный заряд и становится анионом.
Таким образом, ионная связь — это связь, образованная за счет электростатического притяжения катионов к анионам.
Образование такого типа связи характерно при взаимодействии атомов типичных металлов и типичных неметаллов.
Например, фторид калия. Катион калия получается в результате отрыва от нейтрального атома одного электрона, а ион фтора образуется при присоединении к атому фтора одного электрона:
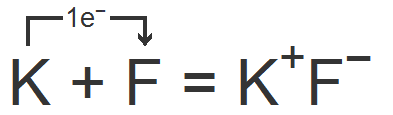
Между получившимися ионами возникает сила электростатического притяжения, в результате чего образуется ионное соединение.
При образовании химической связи электроны от атома натрия перешли к атому хлора и образовались противоположно заряженные ионы, которые имеют завершенный внешний энергетический уровень.
Установлено, что электроны от атома металла не отрываются полностью, а лишь смещаются в сторону атома хлора, как в ковалентной связи.
Большинство бинарных соединений, которые содержат атомы металлов, являются ионными. Например, оксиды, галогениды, сульфиды, нитриды.
Ионная связь возникает также между простыми катионами и простыми анионами (F−, Cl−, S2-), а также между простыми катионами и сложными анионами (NO3−, SO42-, PO43-, OH−). Поэтому к ионным соединениям относят соли и основания (Na2SO4, Cu(NO3)2, (NH4)2SO4), Ca(OH)2, NaOH).
Данный тип связи образуется в металлах.
У атомов всех металлов на внешнем электронном слое присутствуют электроны, имеющие низкую энергию связи с ядром атома. Для большинства металлов, энергетически выгодным является процесс потери внешних электронов.
Ввиду такого слабого взаимодействия с ядром эти электроны в металлах весьма подвижны и в каждом кристалле металла непрерывно происходит следующий процесс:
М0 — ne− = Mn+ , где М0 – нейтральный атом металла, а Mn+ катион этого же металла. На рисунке ниже представлена иллюстрация происходящих процессов.
То есть по кристаллу металла «носятся» электроны, отсоединяясь от одного атома металла, образуя из него катион, присоединяясь к другому катиону, образуя нейтральный атом. Такое явление получило название “электронный ветер”, а совокупность свободных электронов в кристалле атома неметалла назвали “электронный газ”. Подобный тип взаимодействия между атомами металлов назвали металлической связью.
Если атом водорода в каком-либо веществе связан с элементом с высокой электроотрицательностью (азотом, кислородом или фтором), для такого вещества характерно такое явление, как водородная связь.
Поскольку атом водорода связан с электроотрицательным атомом, на атоме водорода образуется частичный положительный заряд, а на атоме электроотрицательного элемента — частичный отрицательный. В связи с этим становится возможным электростатическое притяжения между частично положительно заряженным атомом водорода одной молекулы и электроотрицательным атомом другой. Например водородная связь наблюдается для молекул воды:
Именно водородной связью объясняется аномально высокая температура плавления воды. Кроме воды, также прочные водородные связи образуются в таких веществах, как фтороводород, аммиак, кислородсодержащие кислоты, фенолы, спирты, амины.

Добрый день. Можно прояснить ситуацию по поводу хлорида алюминия и оксида алюминия?
Хлорид алюминия — химическая связь ковалентная полярная, значит, кристаллическая решетка атомная?
Оксид алюминия — кристаллическая решетка атомная, а химическая связь — ионная или ковалентная полярная?
Здравствуйте, Елена. Прошерстив все зпадания банка ФИПИ, касающихся типов связи, могу сказать, что сдающим полезнее считать, что во всех веществах металл-неметалл следует имеет место ионный тип связи.
Тем не менее, Вы правы, есть исключения.
Однако, из всего списка заданий ЕГЭ банка ФИПИ на связи (около 160) мне, из веществ, не попадающих пол написанное выше правило, попался только нитрид алюминия. Данное соединение имеет ковалентный тип связи и атомную решетку. Указанный вами хлорид алюминия имеет ковалентный тип связи и молекулярное строение. Оксид алюминия — ковалентная связь, атомная решетка.
Спасибо за ответ. Я, как учитель, сама учу детей по описанному Вами правилу. Вот только иногда разного рода исключения сбивают с толку.
Да. И, у сожалению, в химии таких исключений полно
И можно еще вопрос? Почему в оксиде алюминия связь ковалентная, если разница в элетроотрицательности больше 1,7?
Вообще понятие ионная и ковалентная полярная связь условны, поэтому еще иногда употребляют такое понятие как «степень ионности связи» или «степень ковалентности связи». Абсолютная ионная связь по сути абстракция, в принципе, как и ковалентная и металлическая. Например, в том же хлориде натрия, не смотря на то, что принято считать, что тип связи в нем ионный, в действительности электрон не на 100% принадлежит атому хлора, и, соответственно, не на 100% ушел от атома натрия. То есть даже в этом случае можно говорить о небольшой доле ковалентности связи. То же и в случае оксида алюминия, только в его случае степень ковалентности и степень ионности связи заметнее выражены, чем у того же хлорида натрия.
У хлорида алюминия молекулярное строение? Запуталась…
Здравствуйте! В сборнике Медведева ОГЭ 2022 года считается, что в хлориде алюминия и бромиде железа (III) связь не ионная … Надеюсь не будет таких вопросов на экзамене.
Добрый день! Медведев не является разработчиком экзаменов, не ориентир. Вопросов не будет.
А вот если в Егэ мне попадется вещество AlCl3 то нужно выбрать ковалентно-полярный тип связи или вовсе ионный?
Там ковалентная связь. Однако, спорных ситуаций пока не было. Но могу предложить просматривать все варианты ответа и выбирать наиболее подходящие. В любой ионной связи всегда присутствует доля ковалентной. Поэтому, если стоит задача выбрать ионную связь, надо выбирать соединение состоящее из металла с наиболее выраженными металлическими свойствами и неметалла с наиболее выраженными неметаллическими. В таком соединении будет выше доля ионной составляющей
СO2 это неполярная а у вас написано полярная
как интересно)
и, кстати, правильно написано. Пожалуй, так и останется:)
P.S. Не надо путать понятия полярная/неполярная молекула и полярная/неполярная ковалентная связь.
В школьной программе, как и в вопросах к экзамену, в молекуле PH3 принято считать связь ковалентной неполярной, так как электроотрицательности атомов фосфора и водорода практически одинаковые. Или я не права?
На самом деле там связь фосфине очень мало, но все же полярная
Разъясните, плиз. Как проще понять это: «…внутренняя энергия вещества ниже, чем внутренняя энергия отдельных атомов, из которых оно образовалось». Я сижу и туплю(
Это понятие из физхимии, если ты учишься в школе забей на этот термин и не заморачивайся
Есть такой вывод: Если разность в ОЭО элементов больше 1,7, то связь ионная. Если меньше 1,7, то ковалентная полярная. Считаю, что в тех случаях,когда даются в задании соединения переходных металлов и например, амфотерные соединения , нужно указывать значения ЭО , чтобы была возможность произвести расчеты
Добрый день! Проводить подобные расчеты, равно как и помнить предельные значения для разности в электроотрицательностях элементов школьники не обязаны. Кроме того, существует несколько вариантов шкал ЭО и сразу же возникнет вопрос, какую из них брать. Как выше уже указывал Сергей Иванович, спорных моментов на ЕГЭ не возникало, разобраться можно по-простому.
по то му же SiO2…. в ответах ОГЭ указывается ковалентная полярная связь, ав ответах ЕГЭ уже ковалентная неполярная
Если разговор идет о связи кремний-кислород, то неполярной она не может быть точно. Этот вопрос обсуждению не подлежит даже при простом сравнении свойств двух элементов.
Можно ли использовать для подготовки только этот сайт,не прибегая к профильным учебникам Еремина,Новошинского?
Добрый день! Комбинации этого сайта и курса вебинаров у Сергея Широкопояса вполне будет достаточно.
Смогу ли я,если выложусь на все 100%,написать ЕГЭ на 90+ баллов с помощью Ваших ресурсов и вебинаров?
Добрый день! Если сдавать в этом году, а уровень примерно нулевой, то уже не удастся. На мой взгляд, за оставшееся время реально добавить 30-35 баллов к текущему результату. И это при условии интенсивной и постоянной работы.
Нет,сдавать в 2022 году!Тогда получится?
Тогда есть шанс при должном старании. Пробуем!
Если ионная связь — электростатическое притяжение разноимённо заряженных ионов, то получается, что связь существует при любом расстоянии между ионами. Поскольку это противоречит эксперименту, то вышеуказанное определение принципиально неверно, зато удобно…
Добрый день! Для подготовки к экзамену не всегда имеет смысл вдаваться в высокие материи.
в ацетоне ионное строение?
Добрый день! Молекулярное.
Доброго дня! Подскажите, пожалуйста, какой тип связи и тип кристаллической решетки у карбида алюминия, карбида кальция, карбида натрия и силицида магния?
Добрый день! В рамках ЕГЭ не требуется.
А в KNO³ есть ковалентные связи, образованные по донорно-акцепторному механизму…?
Добрый день! Есть.
Здравствуйте, а между молекулами других галогеноводородов (кроме HF) могут быть водородные связи?
Добрый день! Нет, не могут. Не хватает разницы в электроотрицательности.
Добрый день Скажите пожалуйста ,можно считать что в фтороводороде связь ионная ведь получается ч то разность э.о. между водородом и фторо1.9 а известно что если разность составляет более 1.7 связь считается ионной?
Добрый день! Нет, нельзя.
Здравствуйте . скажите .пожалуйста. какой вид связи будет между углеродом карбоксильной группы и альфа углеродом в кислотах?
Добрый день! В рамках нынешней школы и ЕГЭ будет ковалентная НЕполярная. По жизни, конечно, полюса там есть из-за разного окружения. Поэтому полярная.
Спасибо
Здравствуйте, а характерна ли водородная связь для солей аммония, допустим хлорид аммония там ведь есть связь между водородом и азотом значит связь характерна ???
Добрый день! Наличие ионной связи исключает образование водородных.
Здравствуйте! Какой тип связи в оксиде хрома (VI) и оксиде марганца (IV)?
Добрый день! В реальности связь ближе к ковалентной.
